文|青眼
“复配原料恢复报送了”“太好了,一切又回归正常”“不用再纠结产品的备案问题了”……今日,多位行业人士向青眼透露,“原料安全信息登记平台”已可对复配原料进行报送,这意味着,行业从原料报送到产品备案又回到了正轨。
复配原料报送“悄然”恢复
据多位行业人士介绍,今日上午,登录“原料安全信息登记平台”时发现,在“基本信息和工艺简述”板块的“原料基本信息”填报页面上,多了一个“增加组分”的按钮,点击该按钮进行操作后,发现原料可添加组分。这意味着,复配原料又可以报送了,原料报送恢复到了今年9月3日前的正常操作。
青眼注意到,目前在进行原料报送时,企业仍需输入《已使用化妆品原料目录》中对应原料的序号,该原料的中文名称、INCI名称会自动关联带出,无需输入。但在点击“增加组分”的按钮后,即会显示出,“商品名”“原料组成”等项目,可根据复配原料中的组分进行添加,并填报原料的商品名。
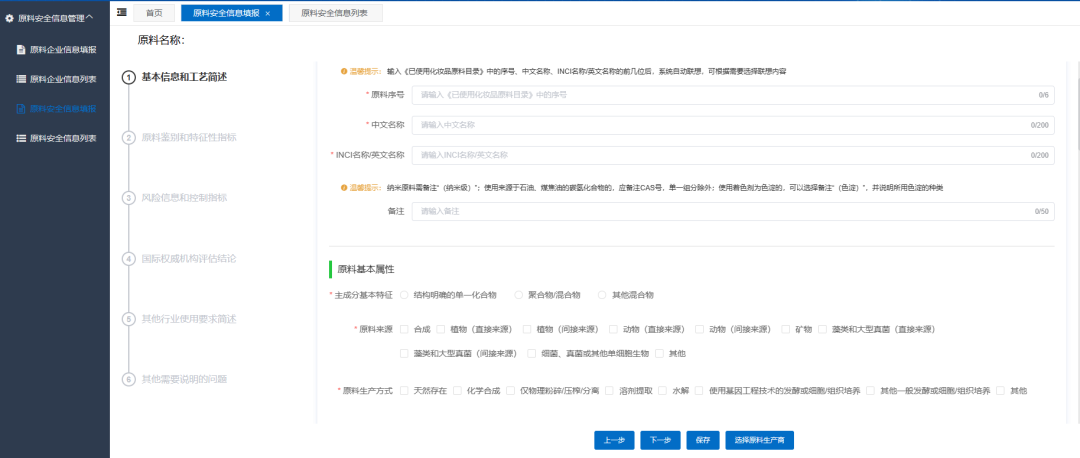
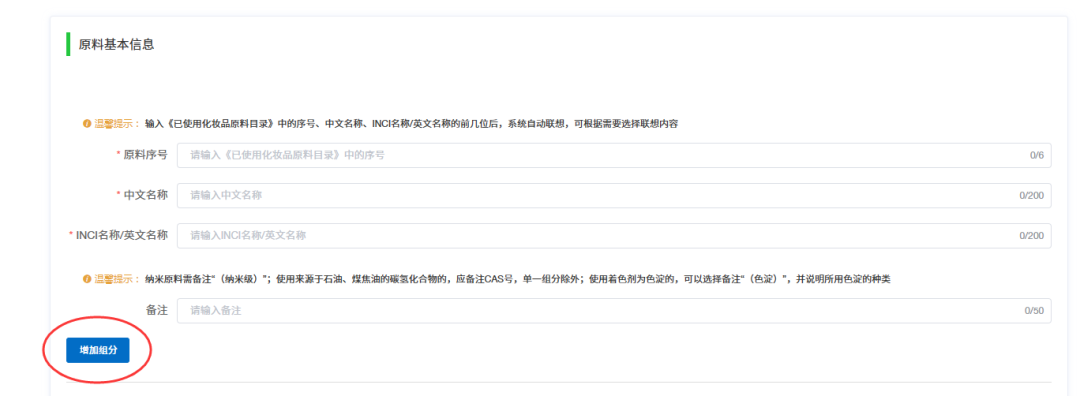
截自“原料安全信息登记平台”(上图为9月6日截图,下图为11月1日截图,受访人供图)

据悉,此次原料报送系统的更新并没有发布公告,因此一开始很多企业都还没发现,直到今日下午,大家才普遍关注到这一变化。
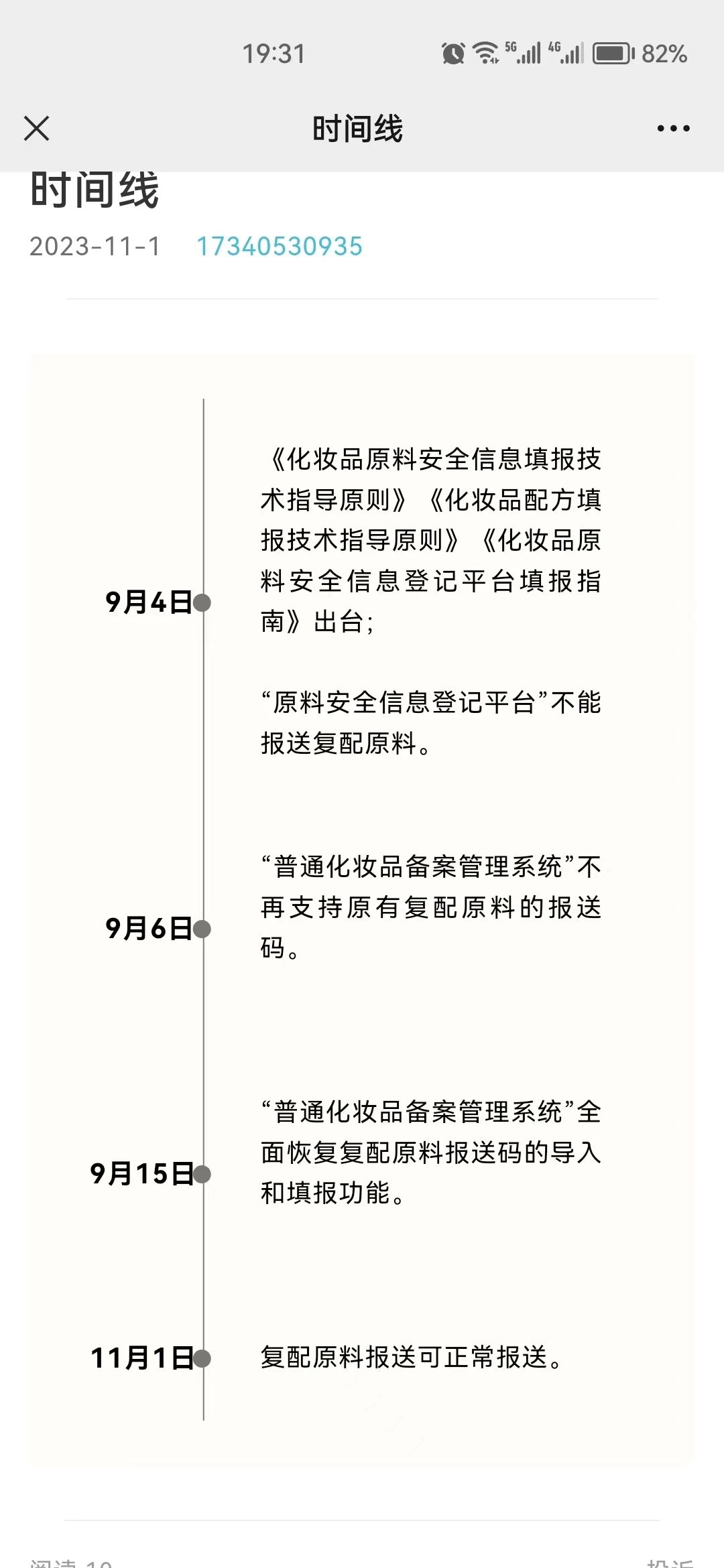
事实上,从9月4日,复配原料不能报送,到“普通化妆品备案管理系统”中不能关联复配原料报送,再到今日一切恢复如初。短短两个月时间里,行业人的心情就如同坐过山车般跌宕起伏,如今“石头”终于落地。
回顾事件始末。9月4日,中检院发布了《化妆品原料安全信息填报技术指导原则》《化妆品配方填报技术指导原则》《化妆品原料安全信息登记平台填报指南》三份文件,并同时对“原料安全信息登记平台”进行了升级。由此,复配原料不能在该平台进行报送,企业所报送的原料必须是《已使用化妆品原料目录》中有独立序号的原料(详见青眼文章《原料报送又有“大地震”!》)。
两天后,“普通化妆品备案管理系统”进行维护更新,且更新后的系统不再支持原有复配原料的报送码。这也标志着,此前已报送的18万+个复配原料报送码就作废了,不能再与化妆品备案系统进行关联。
可喜的是,9月15日,“普通化妆品备案管理系统”再次维护更新后,又全面恢复了此前已有复配原料报送码的导入和填报功能。但这也只是18万+个复配原料报送码再度重启,却依旧没有解决复配原料不能报送这一根本问题。
直至今日,复配原料报送终于恢复如初,今后,企业在进行化妆品备案时也无需再纠结苦恼,正常关联原料报送码即可。
“心中的石头终于落地了”“这下从根本上解决了我们的担忧,一切如旧,我们要开始积极准备所有原料的安全信息资料填报了”……行业人士纷纷说道。
根据国家药监局要求,自明年1月1日起,化妆品注册人/备案人需进行产品配方所使用全部原料的原料安全信息资料填报,显然,留给企业的时间也不多了。
完整版安评也有望延期?
值得关注的是,早在9月15日,“普通化妆品备案管理系统”全面恢复复配原料报送码的导入和填报功能时,即有资深行业人士认为,“监管部门已关注到企业的意见和心声并作出了调整,之后原料报送系统说不定也会调整过来”,并建议“企业先不要自乱阵脚,大家可以先耐心等一等”。如今来看,民有所呼,上有所应。
有行业人士认为,虽然从理论上来看,监管部门通过控制“原料报送平台”的填报,仅允许企业报送《化妆品已使用原料目录》中的原料而不能报送复配原料的初衷,是想快速了解8000多种原料的风险等级和参数,并从源头对化妆品安全把关。“这种想法是很好的,但是却并不符合实际情况。因为,本质上做化妆品和做药品是两回事。很多药都是单一组分,但是化妆品却大多是多组分,没有办法实现仅报送单一组分原料。政策也需要接地气才行。”
另值得关注的是,虽然,原料报送从法规操作层面与完整版安评的执行并无直接关联,但是,经由此事后,也让行业看到了监管部门“考虑企业实际情况并及时调整”的积极因素。因此,不少行业人士认为,“说不定,完整版安评的执行时间也会延迟,毕竟真的太难了,大家都做不到。”
据悉,由于明年5月起企业需提供完整版安评报告,方能进行化妆品注册备案,因此,随着时间临近,这一政策的执行问题也成为了当下行业讨论的重点。
而完整版安评的难度也的确是行业的一大痛点。近日,从青眼调研的情况来看,不少企业均表示“在实践完整版安评报告上显得力不从心”。主要原因即在于毒理学实验成本较高、周期长;以及一些原料需进行动物实验,大量植提原料缺乏毒理学数据,因此,大多企业难以对所有产品与原料进行毒理测试(详见青眼文章《完整版安评,难倒化妆品企业!》)。
因此,不只是中小企业在“喊难”,即便是行业头部企业的负责人也表示,施行完整版安评报告有难度。目前,企业大多处于观望和焦灼的状态中,不敢轻举妄动。
不过,从今日复配原料重新恢复报送一事来看,却又让不少行业人士重新燃起了希望。“目前已经有协会进行反映了,希望此事也能得到监管部门的重视,听听企业的心声,延缓执行的时间。”
对于完整版安评一事,一位不愿具名的法规人士表示,从法规的管理方向来看无疑是正确的,但需要给企业时间。“以1988年出台的《化妆品卫生监督条例》为例,与之配套的《化妆品安全评估技术守则》直到2015年才实施。”在他看来,“从立法的角度来看,肯定是要放眼未来几十年的行业发展,法规从严这是毋庸置疑的。但从执行来看,也要结合行业的实际现状来逐步推进才行。”
此外,还有业内人士建议,对原料风险等级的判断应该由国家牵头制定,企业再结合自身配方进行评估。如果把所有的压力都压在了企业和原料商头上,则不利于行业的发展。
对于完整版安评最终将如何执行,青眼也将持续保持关注。




评论