记者|张乔遇
3月25日晚间,舒泰神(300204.SZ)披露2023年年度报告。
财报显示,2023年公司实现营业收入3.64亿元,比上年减少33.66%;实现归属于上市公司股东的净利润-3.99亿元,同比下滑102.48%,实现归属于上市公司股东的扣除非经常性损益的净利润-4.06亿元,同比下降98.02%。公司研发投入4.48亿元,占营业收入的123.02%,较去年同比增长16.53%。
年报指出,报告期内,受外部环境及行业政策等因素影响,主要产品的销售收入有所下降。
舒泰神以自主知识产权创新药物,特别是生物药物的研发、生产和营销为主要业务,已上市产品包括创新生物药、特色化学药、涉及神经系统、肠道系统等治疗领域。
目前,公司上市销售产品主要为创新生物药物苏肽生(注射用鼠神经生长因子)和特色品种舒泰清(复方聚乙二醇电解质散(IV))及其系列产品。除上述产品外,公司生产销售阿司匹林肠溶片等化学药品。

苏肽生适应症为视神经损伤、正己烷中毒性周围神经病等;舒泰清适应症系用于治疗功能性便秘或术前肠道清洁准备、肠镜及其它检查前的肠道清洁准备等。
报告期内,公司舒泰清实现销售收入1.95亿元,占营业收入的53.59%,较去年同期下降46.48%;苏肽生实现销售收入1.62亿元,占营业收入的44.45%,较去年同期下降6.99%;阿司匹林肠溶片贡献销售收入313万元。
界面新闻记者注意到,2023年公司两款上市销售产品库存量均大幅增长。注射用鼠神经生长因子库存量为50.10万瓶,同比增加321.82%,复方聚乙二醇电解质散(IV)库存量为96.45万瓶,同比增加521.91%。
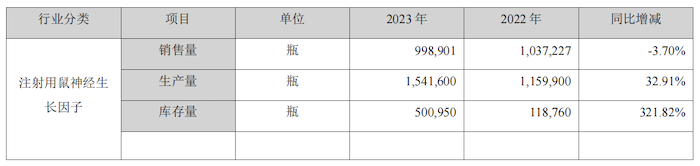
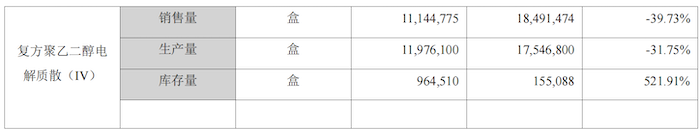
2023年公司在复方聚乙二醇电解质散(IV)方面的生产和销售均出现了下降趋势。然而,值得注意的是,注射用鼠神经生长因子的生产量实现了显著增长,达到了32.91%的增幅,生产总量为154.16万瓶。尽管如此,该产品在同期的销售量却下降了3.7%,仅销售出99.89万瓶。据悉,公司采用以销定产的模式制定生产计划,这种生产增长与销售下降之间的矛盾是何引起?
目前市场上仅4家生产注射用鼠生长因子产品的企业,除了舒泰神的苏肽生,还有未名医药的恩经复、海特生物的金璐捷以及丽珠医药的丽康乐。
自2013年起国内鼠神经生长因子市场迅速扩大,到2016年到到顶峰,市场规模高达33亿元左右,后受医保控费等政策,市场规模不断萎缩,2019年鼠神经生长因子被调出国家医保目录,市场规模再次下跌。
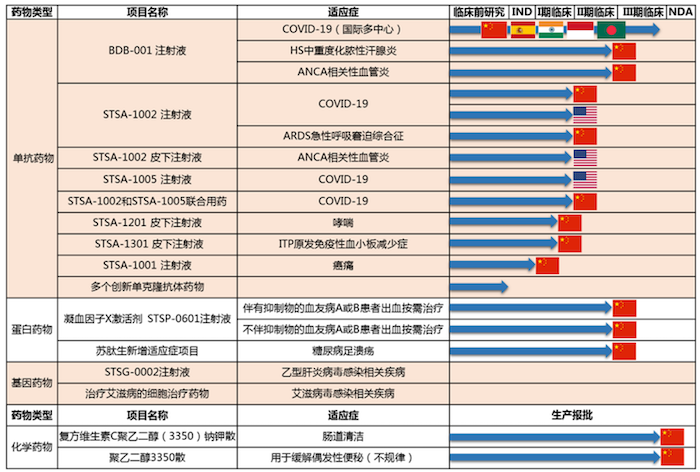
此前,舒泰神开展用于新型冠状病毒感染者所致重症肺炎治疗的临床试验受到市场较多关注。不过,公司近期却终止了BDB-001注射液、STSA-1002注射液、STSA-1005注射液、STSA-1002和STSA-1005联合用药项目在COVID-19适应症方向的研究工作。
据悉,相关研发投入共计3.83亿元。终止原因系基于新冠疫情形势。舒泰神内部人员称,这是基于目前的疫情形势的一个考虑,公司在年报期间跟随审计工作做内部研发项目处理,判断可能商业化价值没有之前那么急切了,因此做出终止的判断。虽然终止了这些药物在新冠方向的适应症的研究工作,其他方向的适应症还会推进。
不过,这已经不是舒泰神第一次终止在研管线了。公告显示,2023年12月公司终止适应症为慢性乙型肝炎的STSG-0002注射液临床试验及后续开发。该注射液为携带靶向HBV基因组P区和X区的shRNA序列表达框的肝嗜性复制缺陷重组腺相关病毒。
舒泰神目前现金流承压,2023年经营活动过产生的现金流量净额-2.28亿元,较2022年减少30.02%。公司期末现金及现金等价物余额已由2022年的2.65亿元减少至8517.70万元。
近期,互联网上传出了舒泰神裁员的消息。年报显示,2023年舒泰神研发人员较2022年减少过半,从262名减少至122名。对于研发人员方面的调整,年报显示系受各方面因素影响,公司对部分早期研发项目及团队进行适度调整,将后续资源投入重点聚焦至临床阶段研发项目的推进。该调整计划有利于公司的持续稳健经营,预期不会对公司日常生产经营活动构成重大不利影响。前述公司内部人员称,研发人员的减少主要是出现在Q3、Q4阶段,截止年报披露时间来看,团队调整已基本到位。
值得注意的是,公司注射用STSP-0601用于伴抑制物的血友病A或B患者出血按需治疗已被纳入突破性治疗品种,已取得Ib/II期临床研究总结报告,正与CDE沟通后续研究及上市申报路径。前述公司内部人员表示,这是目前来看最快上市的在研项目,若后续进展顺利,有望对业绩带来正向提升。




评论