文|氨基观察
两年前,Pan-(K)RAS赛道还在探索阶段,但如今竞赛一再提速。
日前,Kestrel宣布其Pan-(K)RAS抑制剂KST-6051获IND批准,紧接着正大天晴Pan-(K)RAS抑制剂TQB3205也获批临床,竞争再次升温。
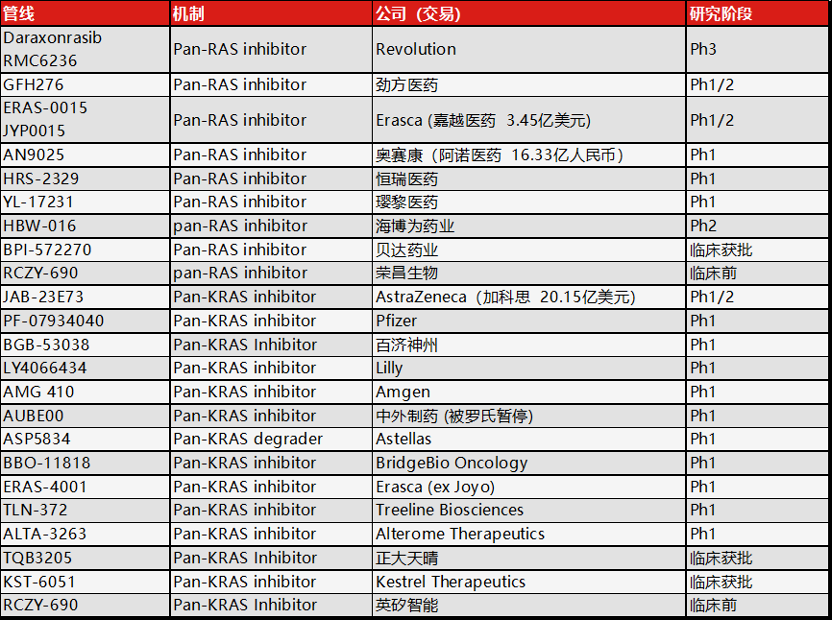
全球共有约20余款Pan-(K)RAS管线进入临床阶段,未来数量仍会被持续刷新。
热潮背后一方面是当前已获批KRAS药物仅针对G12C单一突变,受众群体窄且产生耐药性,临床缺口大。另一方面以Revolution为代表的企业凭借KRAS叙事实现市值一路“飙涨”,以及年初传来的与默沙东的重磅交易,带动了研发热情。
当然了,全球好手蜂拥而至,本质上也代表了一点:Pan-(K)RAS竞赛,已经提前进入下半场,很多分子可能还没开始就已经被淘汰了。
/ 01 /竞争已经开始
虽然还没有成药,但是Pan-(K)RAS的竞赛,已经开始。
在该赛道上,Revolution Medicines是绝对的领跑者。其核心管线Daraxonrasib (RMC-6236)是进度最快的Pan-RAS抑制剂。
早期临床数据显示:在针对二线胰腺导管腺癌(PDAC)的治疗中,RMC-6236治疗KRAS G12X突变患者的6个月生存率达到100%,任意RAS突变患者97%。该结果使其获得FDA突破性疗法认定,用于既往接受治疗的PDAC患者。
同时,Revolution正在加速挺进一线治疗,RMC-9805联合mFOLFIRINOX化疗方案在一线治疗胰腺癌患者1期数据显示ORR为53%。尽管是早期临床,但已为Revolution增添了信心。JPM大会上,公司计划2026开展针对一线肺癌、胰腺癌的3期临床。
值得一提的是,2026年初市场曾传出默沙东拟以约300亿美元收购Revolution的消息。虽然最终双方因估值分歧未达成交易,但这并没有重挫市场信心,反而成为了行业背书。
但Revolution并不是安枕无忧,紧随其后的加科思,就希望发起挑战。
与RMC-6236针对KRAS、HRAS、NRAS不同,JAB‑23E73是小分子抑制剂只抑制KRAS。这也被认为是竞争优势,因为相关研究提示抑制HRAS、NRAS反而会影响肿瘤杀伤作用,还会诱发潜在毒性。
近期JAB‑23E73公布的临床安全性数据似乎验证了这一点。同样是胰腺癌患者,JAB-23E73引发的≥3级TRAEs发生率为14.4%,非头对头临床RMC-6236为34%。在RMC-6236引发的高达91%的皮肤毒性问题上,JAB-23E73诱发率仅为8%,整体安全性可控。
当然了,该结果只是1期研究结果而且是爬坡试验数据,疗效与安全性的竞争优势仍需更大的样本量进行再分析。
只是,RMC-6236与JAB-23E73的争夺,本质上反映了该领域激烈竞争的开始。
/ 02 /被提前的下半场
随着入局者增多,竞争也在继续升级。
虽然新进入临床或IND阶段的分子本质上仍属于Pan-RAS广谱抑制或Pan-(K)RAS选择性抑制两大框架,但分子层面创新不断。
RMC-6236在早期临床中,皮肤毒性和胃肠道毒性较为显著,需要通过剂量优化平衡疗效与安全性。这些挑战,也成为后续竞争者改进设计和策略的重要参考。
同样是分子胶设计,劲方医药的GFH276通过形成CypA‑GFH276‑RAS三元复合物重塑RAS信号,该复合物能抑制多数突变型RAS。在临床前模型中,0.3–3 mg/kg口服剂量即可显著抑制肿瘤,相比RMC‑6236 10 mg/kg,起效剂量更低,且在多重耐药细胞系显示深度MAPK通路抑制。目前GFH276已进入1/2期临床试验,紧跟Revolution脚步。
由嘉越医药授权给Erasca公司的JYP0015同样采用分子胶策略,临床前数据显示,JYP0015对CypA的亲和力较RMC‑6236高出8–21倍,且半衰期更长,是“同类最佳”。其用于PDAC的初步临床疗效数据预计将在今年发布。
阿诺医药的AN9025也是Pan-RAS抑制剂,也声称具有“BIC”潜力。临床前数据显示,AN9025在抑制RAS突变细胞系细胞活力方面效力约为RMC-6236的100倍,药效空间进一步拓宽。
由于专利壁垒和技术门槛,Pan-RAS抑制剂的研发数量相对有限。相比之下,Pan-(K)RAS抑制剂研发节奏明显加快,各家公司纷纷在临床前和早期临床阶段形成了各自独特的“BIC”优势,竞争逐步进入下半场。
在这一赛道中,“ON/OFF”状态双重抑制已是标配。
刚获批临床的KST-6051是一种强效且选择性的KRAS抑制剂,对处于活性(GTP结合)和非活性(GDP结合)状态的KRAS均具有活性。临床前数据显示,KST-6051在多种人类KRAS突变肿瘤模型中均表现出强大的靶向通路调控能力、抗增殖活性以及良好的耐受剂量。
正大天晴的TQB3205同样覆盖两种状态,但其机制不同:通过靶向KRAS上游调控因子SOS1实现广谱抑制。SOS1是一种鸟嘌呤核苷酸交换因子,催化KRAS由GDP结合的失活状态向GTP结合的激活状态转变。TQB3205通过高亲和力结合SOS1,阻断其与KRAS相互作用,从而抑制下游ERK磷酸化信号,最终抑制多种KRAS突变肿瘤细胞增殖。
另一类竞争策略是组合用药,例如百济神州的BGB-53038在已开展的1期安全性试验中,已初步验证了与抗PD-1抗体替雷利珠单抗联合治疗非鳞状非小细胞肺癌,以及与西妥昔单抗联合治疗结直肠癌的疗效。
在Pan-(K)RAS策略中,更激进的方式是蛋白降解,Astellas Pharma的ASP5834就是首款靶向Pan-(K)RAS的蛋白降解剂,可覆盖KRAS G12V/D/C/R/A和G13D突变,以及KRAS野生型基因扩增。通过直接降解KRAS蛋白,该药物实现了更彻底的信号关闭。
新进场的分子在靶向选择性、剂量和安全性策略上做了优化,但绝大多数新机制仍停留在临床早期甚至前临床阶段,谁能真正成为“同类最佳”,还需通过临床试验最终验证。



评论