记者|赵阳戈
眼看过五关斩六将,甚至成功过会的倍特药业,最终却在上市前夕申请撤回,这是怎么回事?

倍特药业IPO受理于2020年7月6日,当年12月17日上会,并成功拿到了"路条",再后来于2021年3月12日提交注册,却在2022年1月11日时,录得“终止注册”的结果。而同期一起上会过会的超捷股份和百洋医药,已经分别在2021年4月27日和2021年5月26日注册生效。
从公开信息看,在2021年9月30日时,倍特药业因IPO注册申请文件中记载的财务资料已过有效期,需要补充提交,程序一度中止。在2021年11月9日公司完成了财务资料更新,程序得以恢复。然而没过多久,2021年12月31日,倍特药业再次因IPO注册申请文件中记载的财务资料已过有效期,需要补充提交,导致程序中止。而这之后的2022年1月4日,公司和保荐机构华泰联合就提交了撤回申请,主动要求撤回注册申请文件,证监会也因此终止了对倍特药业发行注册程序。
这是家怎样的公司?注册稿显示,倍特药业主营业务收入主要来自于制剂类产品销售,在药物类型上涵盖化药制剂、中药制剂,其中公司已上市化学药均为仿制药。在疾病领域上,倍特药业制剂类产品涵盖抗感染类、生殖系统类、心血管类、血液和造血系统类等细分领域多个品种。倍特药业拥有逾210个制剂产品,其中包括16个首仿化学仿制药、17个品规。公司共有16个仿制药产品品规通过一 致性评价,12个产品视同通过一致性评价。一致性评价的产品销售收入占总收入比重在12%左右(2020年前三季度数据)。
2020年前三季度倍特药业的营业收入达到24.87亿元的规模,归属于母公司股东净利润为1.37亿元。计划募资额为9.3亿元。

在上会时,创业板上市委针对倍特药业询问了不少重要问题。比如多个药品中标带量采购,存在中标后价格大幅下降的情形,上市委需要公司明确“两票制”和“集采制”的持续推进对持续经营能力的影响;报告期内倍特药业业务推广费用大幅增长,合作推广服务商数量众多,这方面的合理性也引起了监管层的疑惑;还有就是2020年8月,倍特药业还因侵犯商标为由被其他公司提起了诉讼,诉讼对倍特药业后续影响并不明确,且倍特药业也未就此事项计提预计负债,令事态走向存在未知数,种种都是需要倍特药业给出解释的。
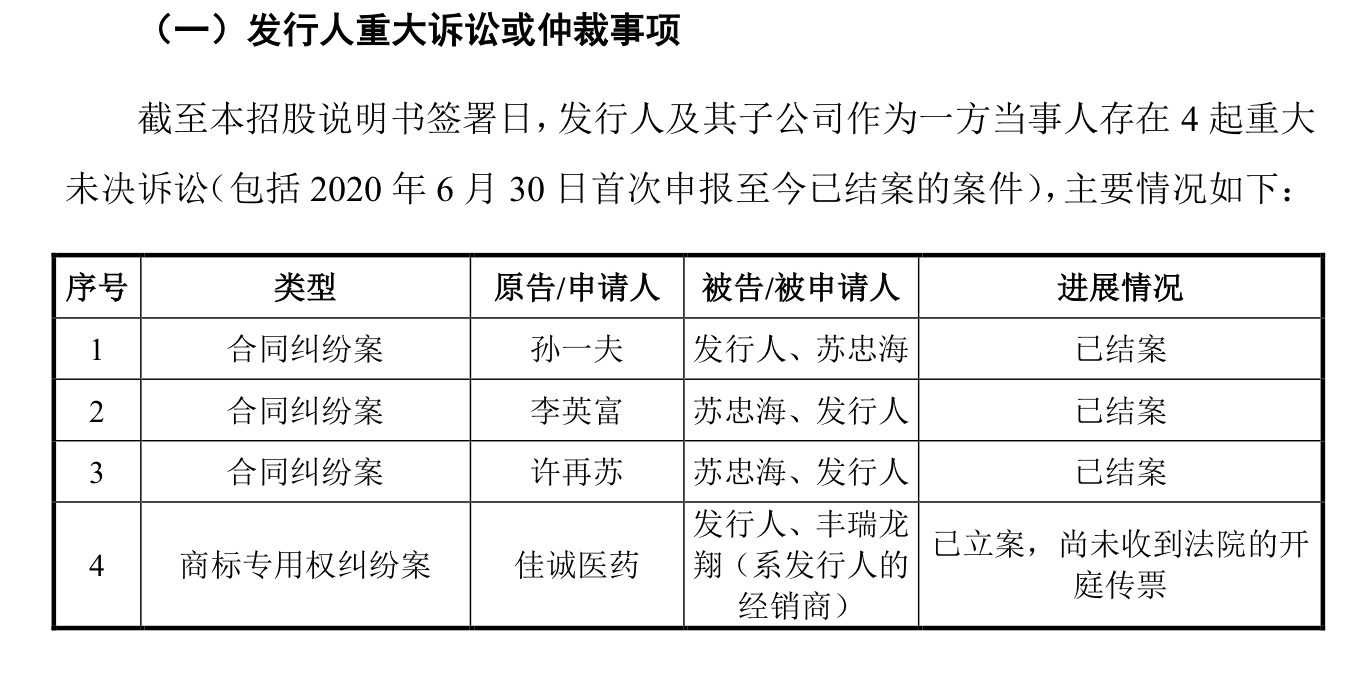
翻开倍特药业的说明书可以看到,公司披露过一起“商标专用权纠纷案”,原告为佳诚医药,被告为倍特药业以及经销商丰瑞龙翔。
据悉,2020年8月,北京佳诚医药有限公司以倍特药业、北京丰瑞龙翔医药有限公司侵犯其商标专用权为由向北京市丰台区人民法院提起民事诉讼,请求判决:认定倍特药业和丰瑞龙翔侵犯佳诚医药注册的第1908229号“捷宁”商标专用权,并责令两位被告立即停止侵权,销毁在市场流通中的侵犯药品的外包装及说明书;倍特药业、丰瑞龙翔共同向佳诚医药赔偿因其侵权行为造成佳诚医药的经济损失共计2400万元及其他诉讼请求。2020年10月10日,北京市丰台区人民法院电话通知倍特药业实际控制人苏忠海相关案件情况。2020年10月12日,倍特药业诉讼律师前往北京市丰台区人民法院自行领取了相关案件的诉讼资料(包括佳诚医药的起诉状和证据材料),法院视为诉讼资料于2020年10月12日送达倍特药业。
对此,根据北京市京大(上海)律师事务所出具的法律意见书,倍特药业对“捷宁” 二字的使用不构成商标侵权。按照倍特药业的说法,氨甲环酸氯化钠注射液的销售收入占其整体销售收入的比例低于1%,也非主要产品。
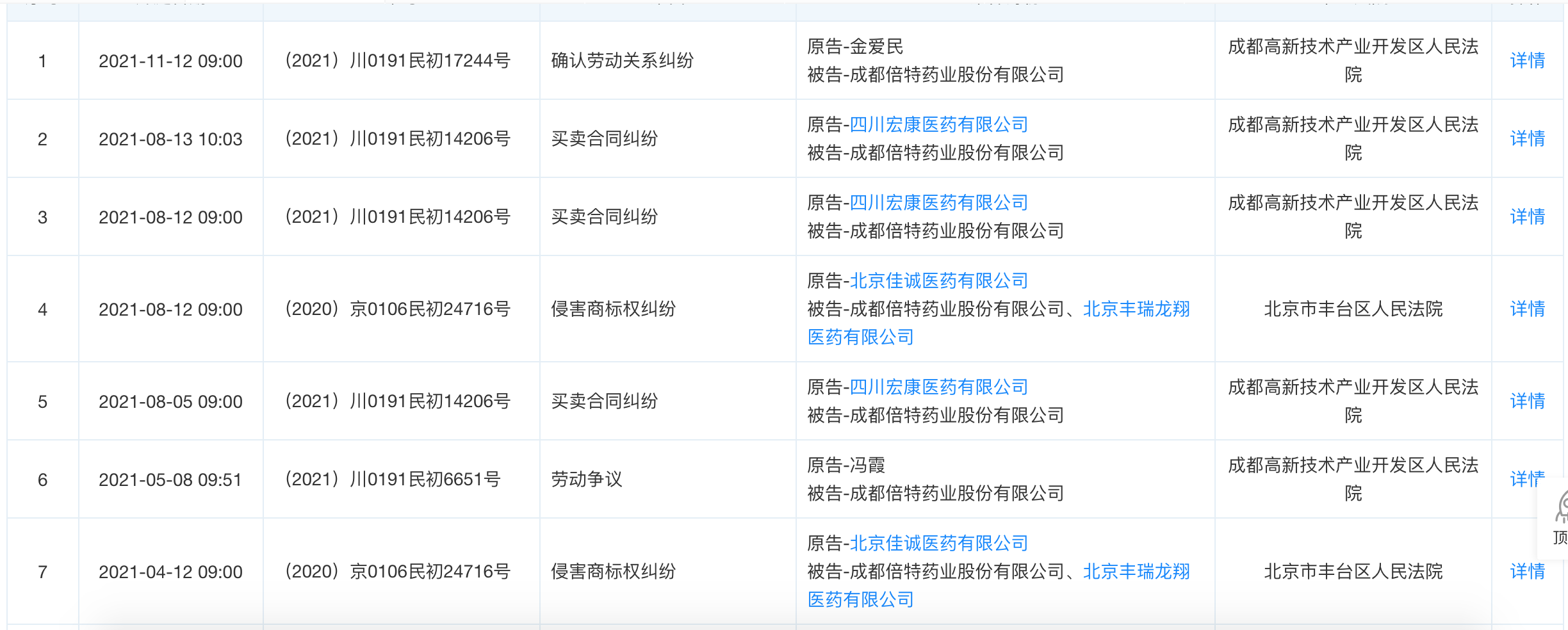
不过需要指出的是,倍特药业在2021年来面对的诉讼不断。根据天眼查显示的开庭公告,2021年11月12日,倍特药业作为被告,有一场劳动关系纠纷;2021年8月份四川宏康医药有限公司作为原告,与倍特药业打了买卖合同官司;上述与佳诚医药之间的纠纷,最近在2021年8月12日还有开庭记录;之后2021年5月又有劳动争议。由于注册稿的日期为2021年3月12日,后续更新的信息也都没有出现在说明书中。

除此外说明书还显示,倍特药业在报告期内存在1起环保行政处罚:2018年子公司仁安药业青白江分公司因未按规定设置排污口而受到成都市青白江生态环境局罚款2万元的行政处罚。同样在2018年,因仁安药业青白江分公司在储存、使用危险品进行生产过程中未采取可靠的安全措施,成都市青白江区安全生产监督管理局对仁安药业作出罚款3万元的行政处罚。2017年9月时,因子公司普锐特药业未按照规定的期限报送代扣代缴、代收代缴税款报告表和有关资料,成都市高新技术产业开发区国家税务局对普锐特药业分别作出“高国税简罚[2017]7729号”、“高国税简罚[2017]7739号”、“高国税简罚[2017]7740号” 行政处罚,各项行政处罚均为罚款50元。
产品质量方面,国家药监局于2020年8月17日发布《关于25批次药品不符合规定的通告》(2020年第55号),提及“经上海市食品药品检验所检验,......标示为海南倍特药业有限公司等公司生产的共3批次注射用奥扎格雷钠不符合规定,不符合规定项目为可见异物。海南倍特系倍特药业的子公司,海南倍特在得知上述事项后,后续也启动了三级召回程序,最终所有市场流通的注射用奥扎格雷钠(规格:80mg,批号:1910211)全部退回海南倍特,共计召回12016瓶。不过后续海南省药品监督管理局对海南倍特该批次奥扎格雷钠注射液留样品进行监督抽检,根据《检验报告》,海南倍特的注射用奥扎格雷钠留样品(规格:80mg,批号1910211)可见异物检验项目检验结果符合规定。




评论