文|推医汇
目前肺癌仍然是全球癌症相关死亡的主要原因之一。即使是早期肺癌,患者的整体生存预后也可能要落后于其他常见类型的早期癌症,如结肠癌、乳腺癌和前列腺癌。由于早期肺癌患者同时存在局部/区域复发或转移复发的可能,因此患者五年生存数据仍不理想。
手术是早期肺癌根治性治疗的重要手段,但是绝大多数患者存在较高的术后复发风险,并因此而失去重要治愈机会。术前/术后给予患者以铂类药物为基础的化疗仅能提高患者五年生存约5%。
如何通过术前系统性药物治疗(新辅助治疗)进一步改善早期肺癌患者的生存预后,降低其术后复发风险呢?近日,Check-Mate 816研究的分析结果重磅公布,为我们带来了好消息!
研究结果显示
术前采用“免疫联合化疗”的新辅助治疗方案对比单用化疗,能显著改善早期(ⅠB期至ⅢA期)可切除非小细胞肺癌(NSCLC)患者的无事件生存期(EFS)和病理学完全缓解(pCR)率,且并不会增加不良事件的发生率或影响接受手术治疗的可行性。
论文作者强调
这项研究系“首次证实Ⅰ~Ⅲ期NSCLC患者在术前化疗的基础上联合免疫治疗能够显著改善预后”。值得关注的是,研究中患者的复发率降低近40%,也就是说有相当比例的患者或能通过术前新辅助免疫治疗进一步实现治愈目标!
相关重要试验结果在2022年美国癌症研究协会年会(AACR 2022)上公布,并同步发表于《新英格兰医学杂志》(NEJM)。
约20%~25%确诊为NSCLC的患者可接受手术切除治疗。
但是近30%~55%的患者在根治性手术治疗后存在复发或最终死亡的可能。
既往研究显示,对于可切除的NSCLC患者而言,在手术的基础上联合术前新辅助以及术后辅助化疗,对比单用手术治疗在五年无复发生存或总生存方面带来的获益十分有限。
不仅如此,很少比例的患者能在术前新辅助化疗方案治疗后出现pCR(即肺部及淋巴结无残余肿瘤细胞)。
通常而言,新辅助治疗后出现病理学完全缓解的患者,其总生存和无进展生存时间显著延长。在肺癌患者的早期临床试验中,基于纳武利尤单抗的新辅助治疗方案显示出可观的临床疗效,并能提高患者病理学完全缓解率。然而,免疫联合化疗新辅助治疗方案的早期临床试验结果仍需大型3期临床试验的数据进一步加以证实。
Check-Mate 816研究是一项国际、标签开放、3期临床试验,旨在评估可切除NSCLC患者接受纳武利尤单抗联合化疗(3个周期)或单独化疗(3个周期)新辅助治疗的安全性和疗效差异。
研究中纳入ⅠB期至ⅢA期可切除NSCLC患者(不存在ALK易位或EGFR突变),并按照1:1的比例随机分配接受纳武利尤单抗(360 mg)联合以铂类药物为基础的化疗,或单用以铂类药物为基础的化疗进行治疗,新辅助治疗3个周期后进行手术切除(新辅助治疗完成后6周内),术后两组患者均接受长达4个周期的辅助化疗、放疗或放疗+化疗。
研究主要终点为EFS和pCR率。关键终点包括主要病理缓解、至死亡或远处转移时间以及患者总生存。此外,研究还对所有接受治疗患者的安全性进行了评估。
结果显示, 2017年3月至2019年11月期间当前研究共招募773例患者,其中505例接受了随机分组,358例患者被分配至纳武利尤单抗联合化疗组(179例)或化疗组(179例),每组176例患者接受了治疗。
在患者至少随访21个月的基础上,研究显示,接受纳武利尤单抗联合化疗方案治疗的患者中位EFS为31.6个月(95%CI,30.2~未达到),接受化疗治疗的患者中位EFS为20.8个月(95%CI,14.0~26.7),两组患者疾病进展、疾病复发或死亡的风险比(HR)为0.63(97.38%CI,0.43~0.91;P=0.005)。
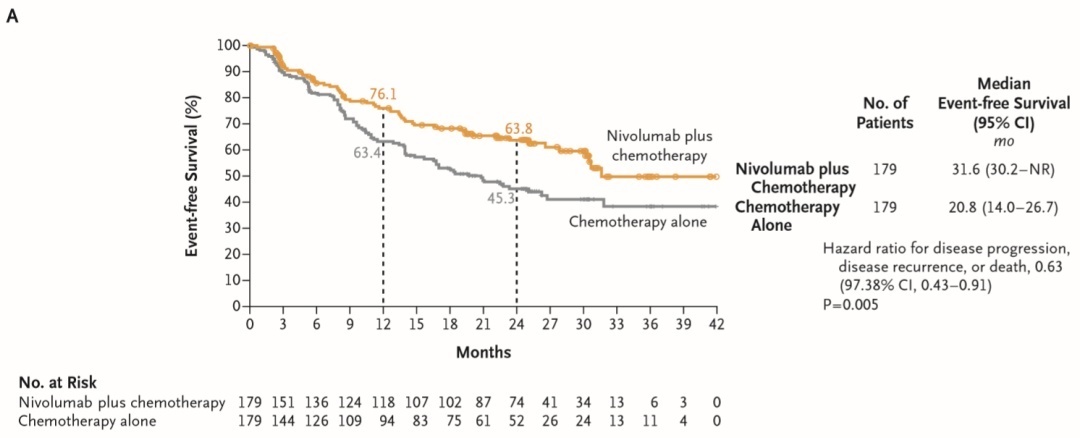
接受不同治疗的两组患者EFS变化
治疗1年后,联合治疗组无进展生存或无复发生存的患者比例约为76.1%,化疗组为63.4%。治疗2年后,预估比例分别为63.8%和45.3%。研究中绝大多数亚组的EFS分析结果均支持纳武利尤单抗联合化疗治疗疗效优于单用化疗。
值得关注的是
分析结果显示,ⅢA期患者对比ⅠB期或Ⅱ期患者,PD-L1表达水平更高(≥1%)的患者对比于PD-L1表达水平较低(<1%)的患者,非鳞癌患者对比鳞癌患者,前者的EFS获益程度要更为显著。
该项研究中,两组患者出现pCR的比例分别为24.0%(95%CI,18.0~31.0)和2.2%(95%CI,0.6~5.6),比值比(OR)为13.94(99%CI,3.49~55.75;P<0.001),且无论患者疾病分期、PD-L1表达或组织学类型如何,研究中所有关键亚组的病pCR分析结果均支持纳武利尤单抗联合化疗治疗疗效优于单用化疗。
此外,联合治疗对比单独化疗,患者的主要病理缓解比例也更高(36.9% vs. 8.9%;OR=5.70;95%CI,3.16~10.26)。
在首次预设中期分析中,两组治疗组患者的中位总生存数据尚未可得,死亡风险比为0.57(99.67%CI,0.30~1.07),虽然未达到显著性差异标准,但显示出潜在获益趋势。
在接受随机分组的患者中,纳武利尤单抗联合化疗组和化疗组中分别有83.2%和75.4%的患者接受了手术。与单独化疗相比,联合治疗组患者微创手术更常见,肺切除术更少见,未观察两组患者手术延迟,治疗相关不良事件的发生数量存在明显差异。
安全性方面,纳武利尤单抗联合化疗组和单用化疗组患者分别有33.5%和36.9%出现3级或4级治疗相关不良事件。
总体而言,研究结果证实:
纳武利尤单抗联合化疗新辅助治疗方案对比单用化疗,能显著延长可切除NSCLC患者的EFS,降低患者疾病进展、复发或相关死亡的风险达到37%。与此同时,免疫+化疗新辅助组合提高了患者的pCR率,即从2.2%提高至24.0%,提高近14倍!
此外,其他关键预后指标,如总生存、至死亡或远处转移时间、主要病理缓解等,分析结果也均支持纳武利尤单抗联合化疗治疗疗效优于单用化疗。安全性方面,在新辅助化疗的基础上联合使用纳武利尤单抗并未增加患者不良事件的发生率,也并未影响患者手术的可行性。
值得关注的是,探索性分析发现,患者治疗前ctDNA水平或可作为术后疾病复发的潜在预测因子,术前新辅助治疗如果能够更好地清除患者体循环中的ctDNA,那么患者或许能够取得更好的预后结果。
论文同期评论指出,目前早期肺癌的治疗仍存在巨大挑战,而新辅助治疗在早期肺癌中的成功探索预示着肺癌治疗新纪元的到来,如果我们能够将免疫联合治疗方案与抗肿瘤疗效评估(如病理学完全缓解评估)有机结合在一起,那么未来将有望进一步降低早期肺癌相关死亡。
参考文献
[1] Patrick M. Forde, et al. Neoadjuvant PD-1 Blockade in Resectable Lung Cancer (May 24, 2018), N Engl J Med 2018; 378:1976-1986. DOI: 10.1056/NEJMoa2202170



评论