界面新闻记者 |
随着首款国产新冠口服药尘埃落定,前期参与竞速的研发者正在考虑“另辟蹊径”。
9月13日晚间,前沿生物(688221.SH)发布公告称,公司近日收到国家药监局核准签发的《受理通知书》,雾化吸入用FB2001的药品注册临床试验申请获得受理。据悉,该产品拟用于治疗轻型和普通型新型冠状病毒感染、新型冠状病毒暴露后预防。
值得一提的是,前沿生物研发的用于治疗新冠中重症住院患者的注射用FB2001目前尚处于II/III期临床阶段,若此次申请获批,意味着雾化吸入FB2001针对新冠密接者的暴露后预防正式进入临床试验阶段。受上述消息影响,9月14日上午开盘后,前沿生物股价一度逆势大涨,涨幅超过7%。
公开资料显示,FB2001为前沿生物与中国科学院上海药物研究所、中国科学院武汉病毒研究所共同开发的抗新冠肺炎病毒3CL蛋白酶抑制剂,前沿生物拥有其在全球范围内的临床开发、生产及商业化权利。
从前沿生物的开发策略不难看出,FB2001主要从新冠治疗和预防两端临床需求入手,其中注射用FB2001主要是针对新冠住院患者用药,雾化用FB2001则用于治疗轻型和普通型新冠病毒感染、新冠病毒暴露后预防。

所谓暴露后预防,是指为防止、阻断可能已接触到某种病原体的人因由该病原体引起的感染或者疾病,而进行的药物阻断和预防。就新冠病毒而言,暴露后预防的目标人群即暴露于新冠病毒检测阳性感染者的密接人群,有效的暴露后预防药物可降低目标人群的感染率。
如今,河南真实生物的阿兹夫定已获批上市,抢先一步占据新冠治疗的赛道,对于卡在临床阶段多时的一众竞争者来说,将更多研发的注意力集中于密接者暴露后预防,或不失为良策。
在此之前,上海瑞金医院曾发起过一项IIT研究(研究者发起的临床研究),以此评价雾化吸入FB2001用于新冠密接者暴露后预防的有效性和安全性。前沿生物方面表示,数据表明,FB2001雾化吸入给药,具有预防新冠病毒感染的潜力,前沿生物将积极推进FB2001雾化吸入制剂拟用于暴露后预防的临床研究。
针对临床前的研究,深圳市第三人民医院院长卢洪洲也给予了肯定,他表示,FB2001雾化吸入制剂在动物试验中显示了非常强的降低肺部病毒载量的抗病毒疗效,具有预防新冠病毒感染的潜力。奥密克戎及其变异毒株更倾向于感染人的上呼吸道,雾化吸入给药方式是非常好的切入点,未来在医院、家庭和社会面密切接触者中都具有比较好的应用场景。
截至目前,新冠预防类药物赛道上并非前沿生物独一家。
5月16日,先声药业(02096.HK)曾发布公告称,公司与中国科学院上海药物研究所、武汉病毒研究所合作的抗新型冠状病毒候选药物SIM0417已获得国家药品监督管理局签发的药物临床试验批准通知书,拟用于曾暴露于新冠检测阳性感染者的密接人群的暴露后预防治疗。SIM0417系国内首个正式进入临床试验阶段的用于密接暴露后预防的新冠研发药物。
根据先声药业8月31日发布的半年报,SIM0417对比安慰剂用于新冠病毒感染人群、新冠阳性感染者密接人群暴露后预防的2项临床试验正在多个省市开展,已进入临床II/III期阶段。
而在适用范围更广的新冠预防药物领域,由阿斯利康研发的“恩适得”作为全球唯一一款获批上市的新冠预防药物,目前已在众多地区获批暴露前使用,并于今年7月落地海南博鳌先行区。紧接着,药明生物(02269.HK)宣布,公司与阿斯利康就恩适得的本地化生产达成战略合作。
然而,无论从实际疗效还是市场规模,新冠预防类药物并不被业界一致看好。
从作用机理来看,病毒学专家接受界面新闻采访时表示,对于新冠病毒而言,很难制成暴露后预防的药物,原因在于:一方面从病毒看,新冠病毒表面的S蛋白对人细胞表面的ACE2结合力太强,新冠病毒的感染速度太快,不是艾滋病病毒能比的,难以阻断;另一方面,小分子药物来做暴露后预防是不现实的,其药物浓度难以达到阻断效果需要的水平。简单来说,目前只有疫苗接种后形成的中和抗体才是有效的。
而对于恩适得的本土化生产,海南博鳌医疗科技有限公司总经理邓之东曾对媒体表示,“恩适得”作为针对新冠病毒的长效中和抗体,目前在国内主要用于免疫功能受损或免疫力弱群体的预防,该部分群体规模小,占总人群的比例不到2%,而且价格昂贵,真正的预约量很小。
邓之东认为,目前国内疫苗已大面积接种,新冠药物也在陆续审批上市,“恩适得”针对免疫功能受损人群用药的具体政策规定还有待细化,这些都进一步挤压和限制了“恩适得”的发展空间,难以在国内市场形成畅销之势。
界面新闻注意到,为了推进FB2001临床试验,前沿生物原本计划定增募资2.7亿元,该申请已于7月31日获得上交所审核通过。不过值得一提的是,根据前沿生物9月8日披露的《以简易程序向特定对象发行股票发行情况报告书》,此次第一大发行对象杰正投资集团有限公司(下称“杰正投资”)“临阵脱逃”,导致最终募集资金缩水至2亿元。
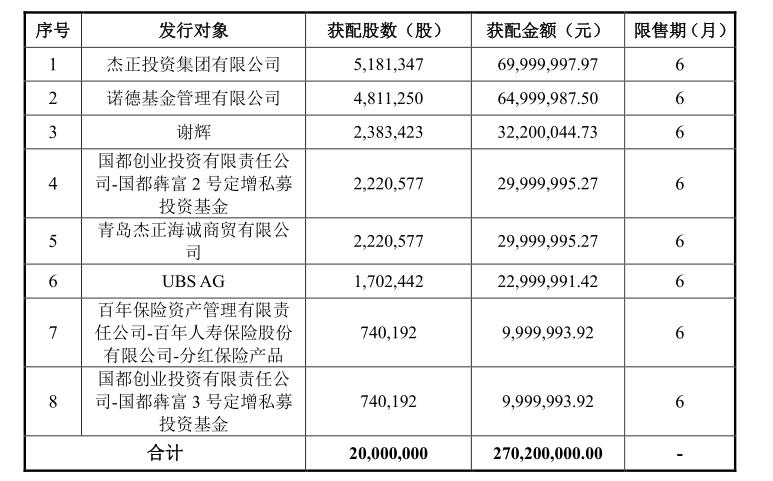
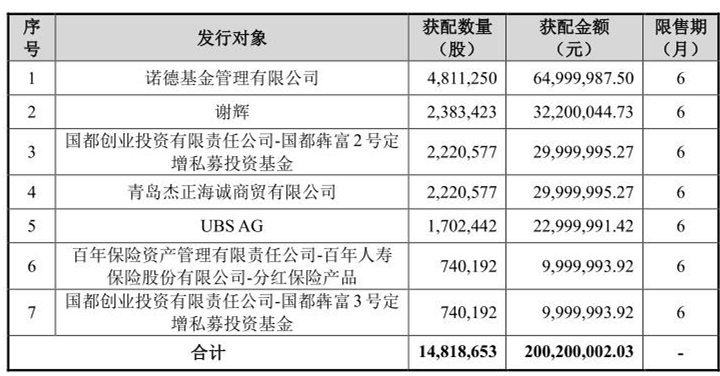
根据发行情况报告书,本次发行价格为13.51元/股,获配第一大投资者杰正投资因未在规定时间内完成缴款,发行人已经终止该协议,且杰正投资缴纳的200万元保证金不予返还。
从杰正投资获配股数量来看,若此次申购成功,便可以跻身前沿生物的第十大股东。如若加上第五大发行对象青岛杰正海诚商贸有限公司的获配数量(海诚商贸系杰正投资子公司,实控人均为方海晖),其合计控股比例将使其成为第九大股东。然而,杰正投资最终选择了主动放弃。
对此,前沿生物证券事务代表对界面新闻表示,杰正投资没有在期限内完成缴款,可能是其自身的资金周转情况出了些问题。
定增缩水是否影响后续临床试验的开展?上述前沿生物证券事务代表表示,“没有影响,公司还有其他资金渠道支撑整个临床进展,因为除了募集资金,公司还有一些自有资金,包括银行信贷、政府补助等“。




评论