【新药界,是界面新闻新近推出的新药点评栏目,立足商业视角,解读上市新药。】
记者 |
编辑 | 任悠悠
在美股的生物医药板块上时不时能看到以下现象:当一家药企一项重磅产品的临床试验“揭盲”后,伴随着结果的悲或喜,这家公司的股价也会大跌或大涨,较近期的如某知名药企的阿尔茨海默症药物研发失败后股价大跌了30%。
今年5月9日,这一幕再次出现。
当日,珐博进(FibroGen)和阿斯利康(AstraZeneca)联合公布了其慢性肾脏病性贫血首创疗法Roxadustat(罗沙司他)的安全性结果,随后珐博进股价急剧跳水,跌幅超过26%,并在此后两个交易日继续下跌至年内低点。
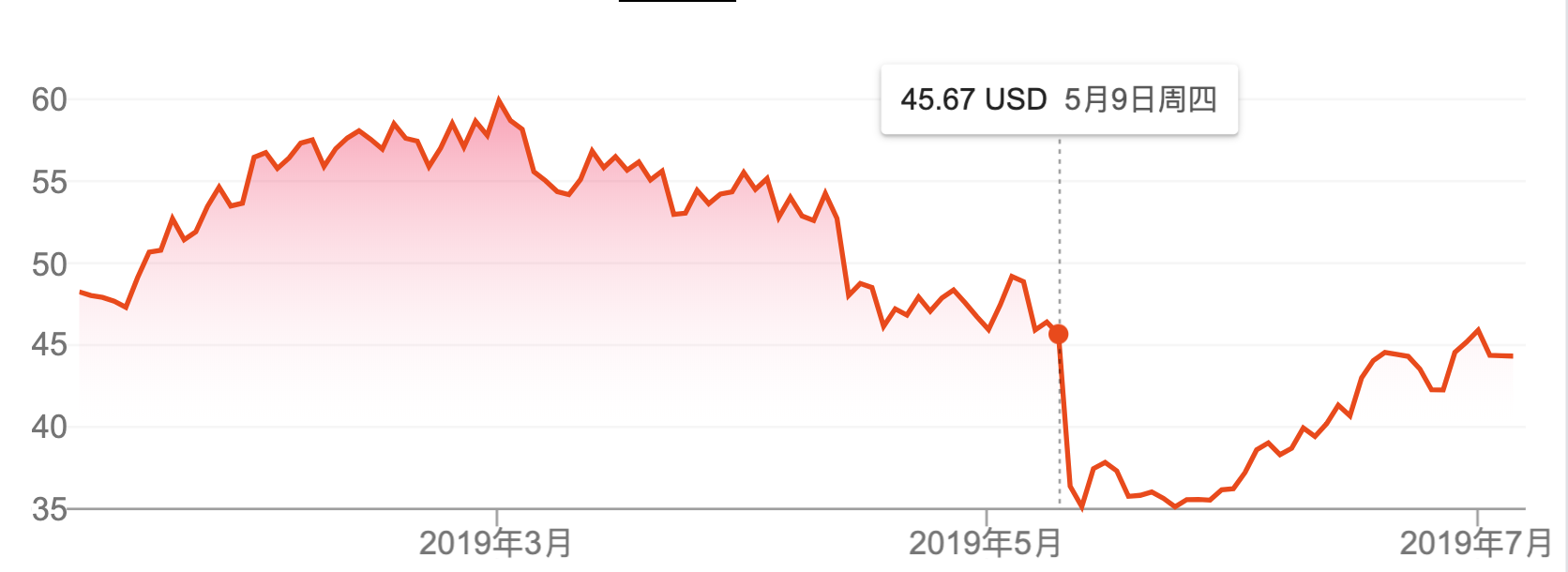
作为首款全球研发,中国率先孵化并已获批上市的国产I类原创新药,罗沙司他的表现自然牵动着大众的神经。

此次股价大跌的主要原因是在本次公布的罗沙司他7项临床试验安全性数据中,美国食品药品监督管理局(FDA)所认可的主要不良心血管事件(MACE)仅获得"没有临床意义上的差异"的结论。
也就是说,与现有的常规治疗手段促红细胞生成素(rHuEPO)相比,罗沙司他在FDA对心血管副作用的认定标准之下并未体现出优势。
华尔街的分析师们认为,这将为罗沙司他在美国的上市及后续市场情况增添许多不确定性,未来可能需要企业、监管部门、医院与市场各方进行再评估。
肾性贫血三十年以来的首款新药
时间回拨到2018年12月,当国家药品监督管理局(NMPA)以优先审评审批通过罗沙司他(国内商品名:爱瑞卓)用于治疗正在接受透析治疗的患者因慢性肾脏病(CKD)引起的贫血时,该药品还尚未在其他任何国家上市。作为国内肾性贫血领域30年来首款新药,罗沙司他在国内临床应用与新药上市的象征性上兼具标志性意义。
此前三十年时间里,肾性贫血领域并未有真正意义上的新药物出现,复旦大学肾脏研究所所长,复旦大学华山医院终身教授林善锬教授此前曾表示,该药品有望让中国肾脏科领域“彻底翻身”。
作为全球首个低氧诱导因子脯氨酰羟化酶抑制剂(HIF-PHI),罗沙司他的作用机理是通过抑制低氧诱导因子(HIF)的泛素化降解,促进内源性促红细胞生成素生成,改善铁的吸收,降低铁调素。在慢性肾脏病患者的多个亚群中,罗沙司他能够维持红细胞生成素水平处于或接近正常生理范围,进而增加红细胞数量,同时不受炎症状态影响,也可避免静脉补铁。
珐博进是罗沙司他的研发发起人,其与阿斯利康达成合作在美国、中国及其他市场共同开展罗沙司他用于慢性肾脏病患者贫血治疗的开发及上市推广工作。阿斯利康和珐博进合作在中国开展罗沙司他的研发项目和商业化活动。
罗沙司他在国内共有20mg与50mg两种规格,根据药品说明书,患者根据体重选择起始剂量:透析患者为每次100mg ( 45-60kg )或120mg( ≥60kg),通过口服给药每周三次(TIW)。研究显示进食不会显著影响罗沙司他的暴露量,因此可空腹服用或与食物同服。对于正在接受血液透析或腹膜透析的患者,可在透析治疗前后的任何时间服用罗沙司他。
今年4月,在药品尚未实现商业上市前,罗沙司他就已先行启动赠药项目,计划将覆盖3万名接受透析的肾性贫血患者。
有关罗沙司他的临床试验一直未停止。
目前,仅针对肾性贫血这一适应症罗沙司他在全球就开展了16项III期临床试验,包括8项在美国与欧盟进行(7项已完成)、2项在中国(已完成)、6项在日本进行(4项已完成),而上述已完成的临床试验都达到了主要疗效终点。
阿斯利康对界面新闻介绍称,本次罗沙司他全球III期研究项目由阿斯利康、珐博进和安斯泰来共同实施,样本来自50多个国家,总量高达9000多名患者。本次试验为心血管安全性评估,是罗沙司总体收益-风险评估的一部分。
在所有患者中,1500名初始非稳定期透析患者在使用了罗沙司他和阿法依泊汀之后,结果显示前者的有效性比后者更显著。4300多名非透析患者的试验效果显示,罗沙司他与安慰剂相比更具有效性,其可通过减缓肾小球滤过率(eGFR)降低的速度延缓肾功能下降。
这本是令人振奋的消息,但5月9日在罗沙司他临床试验安全性数据公布后,FDA后续对罗沙司他的态度是否会波及到中国市场,不禁令人心中充满疑问。
临床安全性数据上的“争议”
根据5月9日的安全性数据,罗沙司他在美国与欧美已完成7项临床试验。这7项试验中,罗沙司他在欧盟药监局(EMA)认可的主要不良心血管事件、心衰和不稳定性心绞痛(MACE+)上达到"非劣效性"(95% CI),在FDA认可的主要不良心血管事件(MACE)得到"没有临床意义上的差异"的结论。
MACE+是指全因死亡、卒中、心肌梗死事件以及因心衰或者不稳定心绞痛需要住院的复合终点;MACE是指全因死亡、卒中和心肌梗死事件的复合终点,是FDA认可的关键心血管安全性终点之一。
以上结果换而言之,与常规治疗手段促红细胞生成素(rHuEPO)相比,对EMA而言,罗沙司他安全性同等或更优;面向FDA时罗沙司他的安全性或好或差。
在一次与投资人的电话会议中,珐博进的CEO Thomas Neff提到,与传统的肾性贫血药物阿法依伯汀(EPO)或红细胞生成刺激剂(ESA)相比,珐博进和FDA在罗沙司他安全性的"非劣效性"上还未达成一致,这意味着罗沙司他的安全性可能会有比目前公布的更负面的结论。
阿斯利康方面对界面新闻回应称,在罗沙司他对心血管安全性汇总分析中,其安全性主要基于III期临床项目中的心血管安全性分析,包括MACE(不良心血管事件)和MACE+(由MACE加上需要住院治疗的不稳定性心绞痛和需要住院治疗的心力衰竭组)的分析结果。总体而言,这些分析将通过评估罗沙司他整体的证据情况来评估罗沙司他的总体效益风险概况,以避免单组试验分析可能存在的偏差。
同时业内人士也认为,"没有临床意义上的差异"的结论相对模糊。
“目前公布的罗沙司他pooled analysis(汇总分析)结果其实是积极的。”阿斯利康表示。
在安全性上,罗沙司他和安慰剂相比无显著性差异。在4000多名稳定透析患者中,罗沙司他的安全性和阿法依伯汀相比无显著性差异。总体上,罗沙司他的有效性和安全性显著,且在其他方面仍存在巨大优势。
从目前公布的数据看,约4000例已透析CKD患者的数据显示,首次发生MACE+的相对风险的95% CI(置信区间)的上限小于预先设定的非劣效性界限。据此认为,罗沙司他与阿法依泊汀的MACE风险在这类患者群体中没有临床意义上的差异;1500多例新发透析CKD患者数据显示,在首次出现MACE+事件这一指标上,罗沙司他优于EPO。
而在MACE安全性方面,相比EPO,罗沙司他具有降低MACE心血管风险的趋势;另外4300多例非透析慢CKD患者数据显示,罗沙司他与安慰剂相比在首次发生MACE+方面的安全性为非劣效性。罗沙司他与安慰剂在MACE风险方面没有临床意义差异。
换句话说,罗沙司他在新发透析CKD患者中的MACE+风险优于标准疗法EPO,MACE风险趋向优于EPO:即可以降低新发ID-CKD患者的心血管风险;在未透析CKD患者的MACE+安全性都小于糖尿病药物心血管安全的1.3非劣效界值;在透析CKD和未透析CKD患者的MACE安全性于标准疗法相比无临床意义的差异。
值得一提的是,1.3的非劣效界值也是FDA在文迪雅事件后所采用的针对糖尿病药物的心血管安全标准。简单而言,FDA要求药品上市前该数值低于1.8,上市后则要低于1.3;上市前高于1.5低于1.8的需补充大型临床试验,高于1.3低于1.5的需做上市后心血管安全性研究。
需要解释的是,虽然现行常规疗法EPO及其衍生物ESAs总体上是一种安全有效的治疗手段,但由于被发现会增加心血管疾病发生率(尤其是血红蛋白较高人群),在2007年时,FDA给ESAs加上其最严重的上市药品警告形式——黑框警告(black box warning),这也就不难理解为何当罗沙司他在MACE上得到与EPO"没有临床意义上的差异"的结论时会引来更多的关注,甚至是股价上的连锁反应。
但是除了“临床意义”外,还存在着“统计学意义”,此前分析指出,在目前“临床意义”无差异的情况下,“统计学意义”上的结果将很大程度上影响罗沙司他是否需要在欧美开展新的临床试验。
尽管如此,这并不意味着罗沙司他这款第一个在中国率先获批的全球新药将面临被FDA拒之门外的境地,综合疗效、药物经济学、安全数据等各方面考虑,罗沙司他在美国获批的可能性依然较大,其安全性问题有待后续更多数据公布,或是与EPO一样被加上黑框警告加上市后研究。
阿斯利康方面则表示,目前还无法对此(在美国上市情况)进行猜测,但阿斯利康与珐博进将积极主动和有关监管部门沟通,并按其要求对说明书进行调整。一旦有更多更新信息,将及时公布。
中国市场最大挑战“没有先例”
国内流行病学调查资料显示,中国慢性肾脏病患者人数超过1亿,其中超过100万患者为终末期肾病患者,成年人群CKD患病率高达10.8%,贫血治疗率为44.9%,而治疗达标率仅为8.2%。国内一项对肾脏科门诊和住院CKD患者贫血状况的调研显示,CKD1-5期患者贫血患病率依次为:22.0%、37.0%、45.4%、85.1%和98.2%,透析与非透析CKD患者贫血患病率分别为98.2%和52.1%。
整体呈现出知晓率低(12.5%)、治疗率低(非透析39.8%)、达标率低(12.1%)的“三低”现状。
中国医科大学附属第一医院肾内科主任医师、科室副主任范秋灵教授对界面新闻记者介绍,由于长期伴随的恶心、呕血压高等并发症,导致许多肾性贫血患者不敢放开吃肉、喝水、耐力差,工作与生活质量受到严重影响,并且还造成了严重经济负担。
据了解,虽然目前透析等费用基本实现了医保覆盖,患者自费开支一个月不到一千, 但甲状旁腺功能亢进、钙磷骨病等并发症治疗药物多是患者自费,往往并发症治疗一个月需花费3-4千,长期以往患者经济负担很重。研究显示,我国慢性肾脏病患者中,贫血患者全因慢性肾脏病产生的年均直接治疗费用比非贫血患者的增加了4倍。
范秋灵还表示,对于目前ESAs药物的副作用,医生实际应当多与患者交流,确保其知情权,但由于缺乏其他用药选择,这一块往往未能得到临床医生的足够重视。不过由于肾性贫血本身也会引发心血管安全问题,总体看用药肯定是利大于弊的。
在罗沙司他获批之前,肾性贫血治疗手段主要包括:铁剂补充,红细胞生成刺激剂(ESAs)治疗(即注射促红素EPO)以及输血治疗,上述三种传统疗法在疗效、安全性与便利性方面均存在局限。
如口服铁剂会使30%-50%的患者严重的胃肠道反应,静脉补铁则会引起皮疹、潮红、低血压等过敏反应。ESAs则只能解决促红素缺乏的问题,无法改善铁吸收和利用,且容易引起其他并发症,如高血压,癫痫,透析通路血栓和高钾血症等。此外便是心血管风险。另外,注射促红素必须静脉给药或是皮下给药,既带来注射疼痛,导致患者依从性差,又增加治疗成本。而输血治疗对患者容易出现溶血、发热和过敏反应等。同时,输血还存在疾病传播和血液污染的风险。
因此,在疗效与EPO类似或是更优的前提下,安全性本被认为会是罗沙司他一个强有力的市场优势所在。
从2010年到2017年,罗沙司他在中国共进行了I-III期临床试验,其中III期试验中进行了代号为806和808两个临床试验。而国家药品监督管理局对罗沙司他适用于CKD透析患者的药品上市批准主要是依据806的结果。该试验收集了所有关于不良反应和安全性信号,并就其进行汇总和分析且公示在了罗沙司他到说明书上,阿斯利康方面表示,在特别关注的心血管事件结果上,与文献报道发生率比较,罗沙司他临床试验中报告的心血管事件发生率并未高于ESAs类药物。
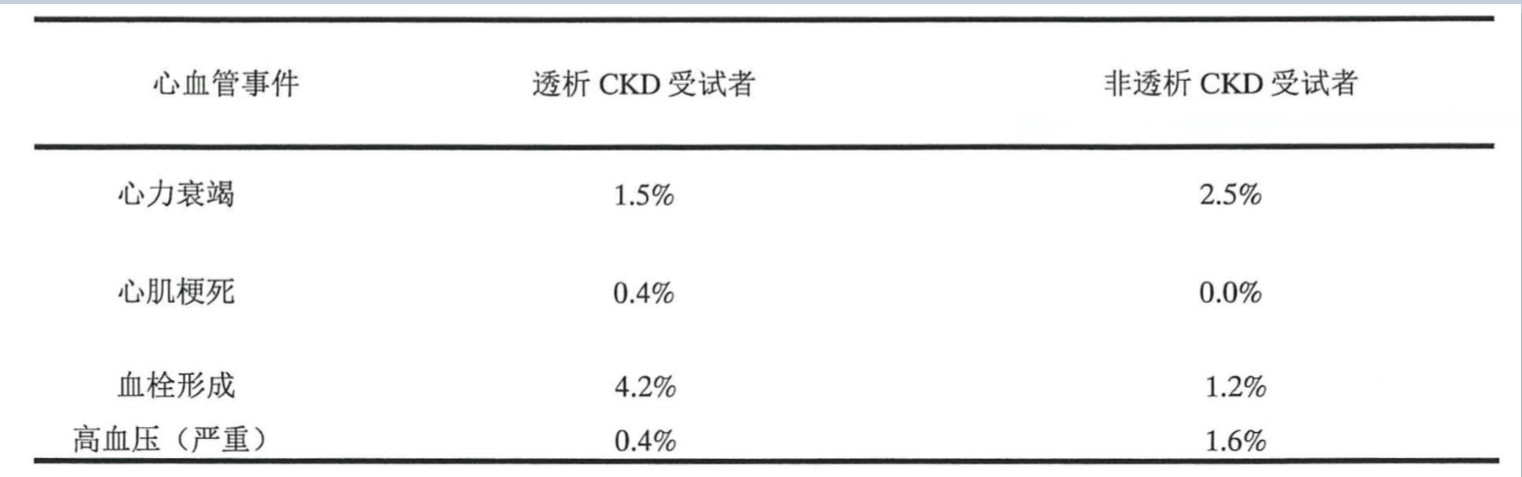
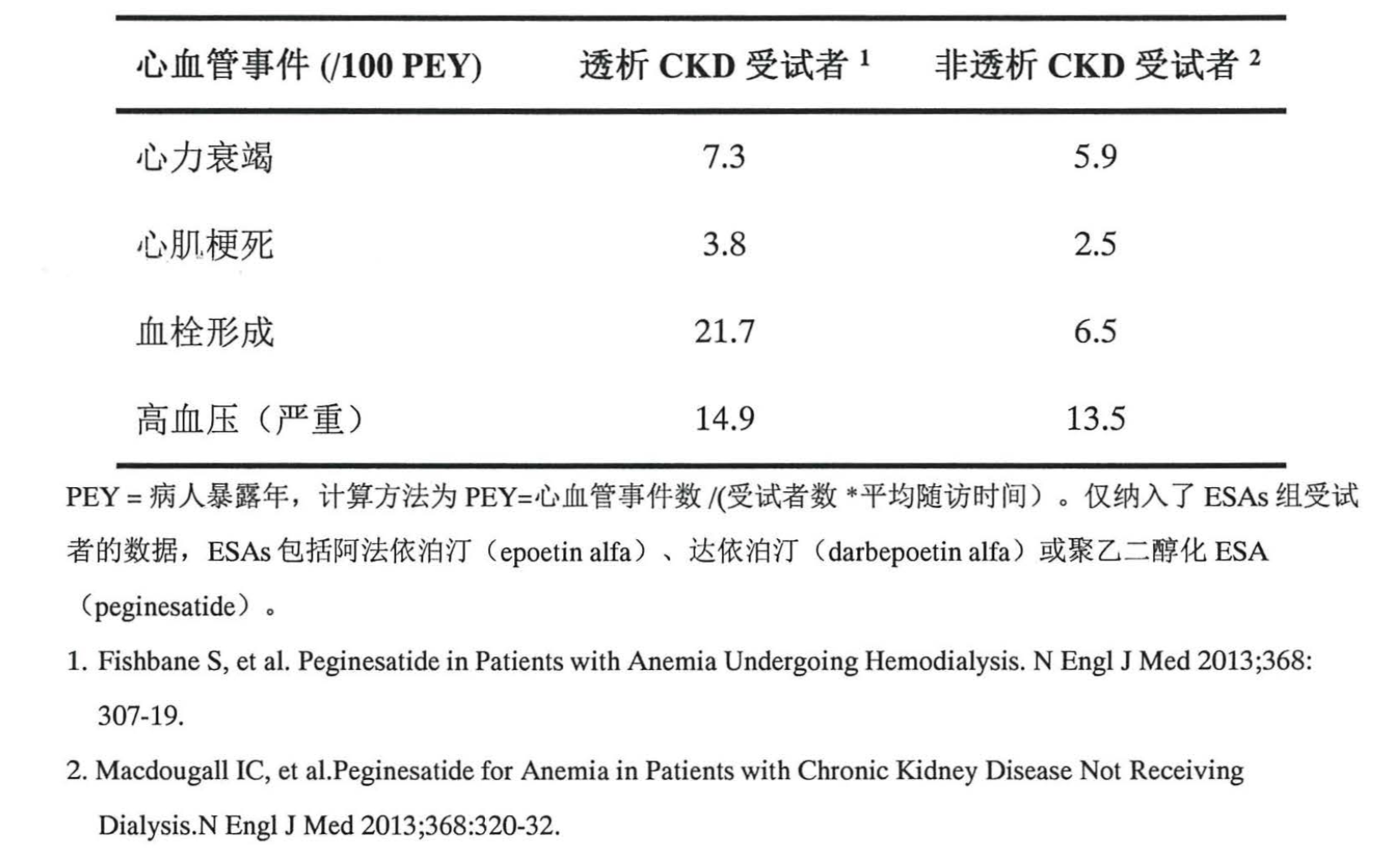
范秋灵认为,如果罗沙司他被FDA加以黑框警告,确实会对国内医生的用药产生很大影响。她介绍,目前临床对EPO的使用就已经很谨慎,而对罗沙司他的发病率不够了解,缺乏足够使用经验,医生会有顾虑。但这并非无法解决,范秋灵希望,可以加大对现有罗沙司他安全性数据的学术推广,给专业医生做细化的讲解分析。她同时也认为,罗沙司他确有其优势所在,患者不会再受炎症影响、EPO抵抗减少,透析患者服用罗沙司他后无需再静脉补铁,这也减轻了经济负担。
阿斯利康中国副总裁,商业战略和卓越运营部负责人,阿斯利康中国首席市场官刘谦在之前的采访中曾提到过:作为全球未上市在中国率先上市的新药,罗沙司他不光在研发上有很多的挑战,在商业上也会有很多的困难。“以前我们做的药都在国外上市了十几年,最少也有四五年,所以我们有大量的国外资料、国外经验,中国模仿剂量、用法,总的来说是一个推广、宣传的过程,学术的过程已经基本上解决了。但是罗沙司他开创了一个前所未有的先例,国外都没有经验,都需要看中国。”刘谦表示。
珐博进中国执行总裁、中国区总经理钟黎蕴华此前也曾对媒体表示,罗沙司他“最难是没有先例”。
与范秋灵的看法接近的是,刘谦此前也表示,罗沙司他的市场计划“要考虑更加偏学术,更加要去探索这个药怎么用是安全的”,如补铁标准、用法和剂量等许多个性化问题还没有解决。
目前,阿斯利康与珐博进已向国家药品监督管理局提交罗沙司他用于CKD非透析患者的上市申请。该申请已进入国家药品审评中心的审核流程中,有望于今年下半年获批。而罗沙司他在美国和欧洲还在进行治疗骨髓异常增生综合征(MDS)贫血症的临床III期试验,及在中国进行临床II/III期MDS贫血症试验。
作为口服胶囊,如后续获批未透析CKD,也可大大加强这部分患者的治疗依从性。
ESAs市场迎来冲击
另有观点则认为,由于美国CKD治疗市场更加成熟,所以在最新的安全性数据出来后,投资人可能会下调罗沙司他在美国市场上的竞争力的预期,这也是珐博进当天股价大跌的因素之一。
范秋灵则表示, 在CKD治疗上,美国市场上有长效EPO,并且对于EPO的调整用量、补铁标准都有统一标准,而这些在国内虽然有指南,但每个医生的操作都不一样。
可以预见的是,罗沙司他将给国内EPO药物带来强劲挑战。
从全球市场看,安进、罗氏、强生与协和麒麟瓜分了ESAs大部分市场,安进于1989年推出了全球第一款EPO药物,2006年全球EPO市场达到峰值126亿美元,此后受到仿制药冲击、FDA黑框警告、美国医保支付改革等因素影响市场体量一路走低,到了2016年滑落至62亿美元左右。
国内市场上,1992年首款进口EPO入华,6年后三生制药首个国产EPO益比奥上市,从2005-2013年,国内样本医院EPO的销售额由1.2亿元增加到3.3亿元,年复合增长率为14%。
目前EPO在国内已是国产仿制药的天下,而三生制药的益比奥在国内样本医院市场自2005年起就占据了半壁江山,随后几年其份额在不断扩大,到2013年,益比奥在国内样本医院的份额达到了65.6%。三生制药2018年年报显示,其两款EPO药物益比奥和赛博尔在2018年合计带来8.97亿元的销售收入,增加4.8%,占到国内EPO市场份额的41%。
而对于三生制药而言,EPO已是其防御型板块,近年的业绩增长主要依靠着治疗血小板减少症的特比澳,该药物2017年进入医保目录后迅速放量,在2018年销售收入大涨71.3%,达到了16.7亿元,IMS数据显示其国内市场份额增至65.3%。
据悉,罗沙司他将在下半年实现商业化上市,目前在国内部分地区招投标进程已进行到报价阶段,也已在多省挂网。以天津为例,根据药剂规格不同,分为498元/盒(50mg)与248/盒(20mg)。医保方面,阿斯利康已与政府相关部门就罗沙司他的医保准入开展积极沟通。
除了罗沙司他外,临床开发中的同类药物还有GSK的GSK1278863、BAYRY的Rolidustat、Akebia的Vadadustat在研,国内恒瑞医药也已于今年4月拿到临床试验批文。
另外,珐博进5月9日跳空的缺口,也在最近补上了。




评论