记者 |
暴力拉升市值逾百亿,新冠疫苗附条件上市能否拯救亏损的康希诺?
2月24日午后,康希诺(688185.SH,06185.HK)股价盘中大幅拉升。
当日午盘,其A股股价报收438.38元/股,跌4.9%;但下午开盘,康希诺的A股股价一度升至515元/股,涨超10%。截至15时收盘,其股价回落至469.60元/股,涨1.87%。当日,康希诺A股市值一度暴涨超130亿元。
与此同时,康希诺港股股价也出现大幅震荡,当日收盘,该股股价至354.2.港元/股,跌4.78%。
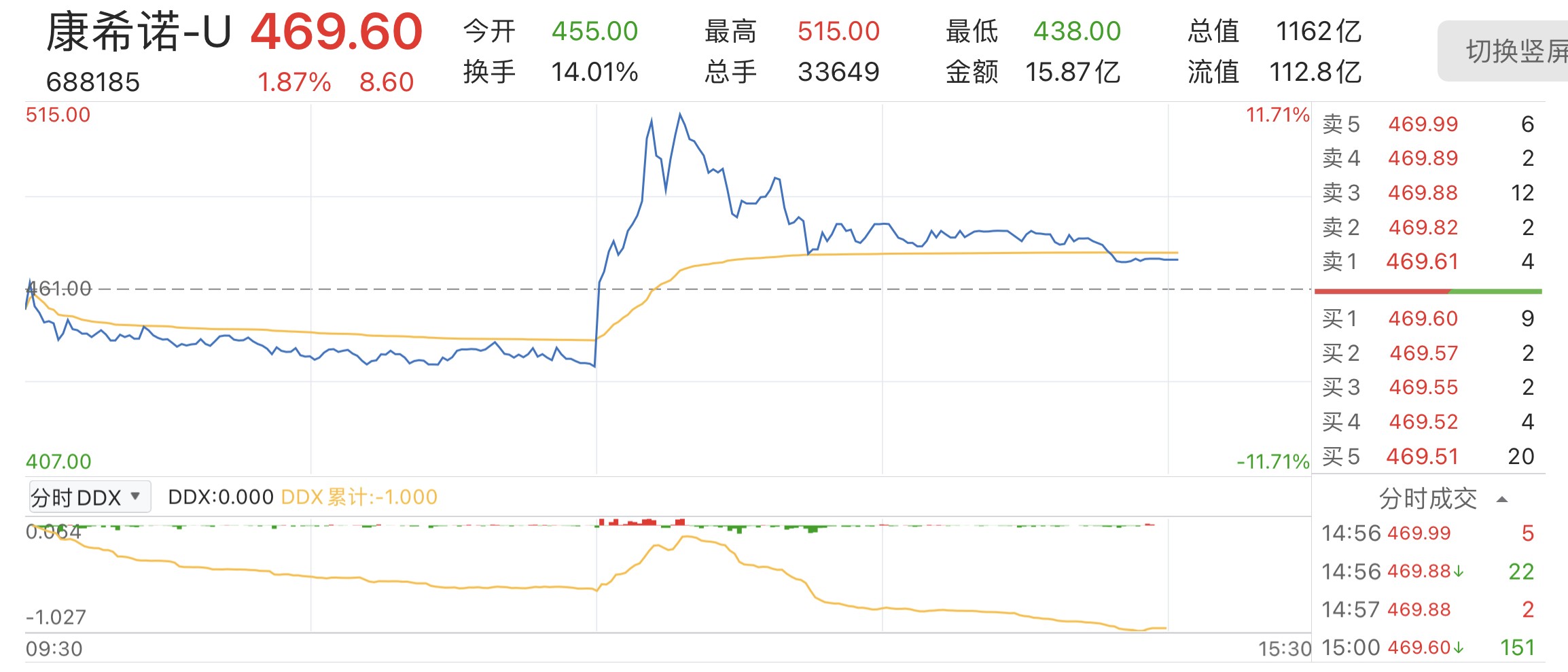
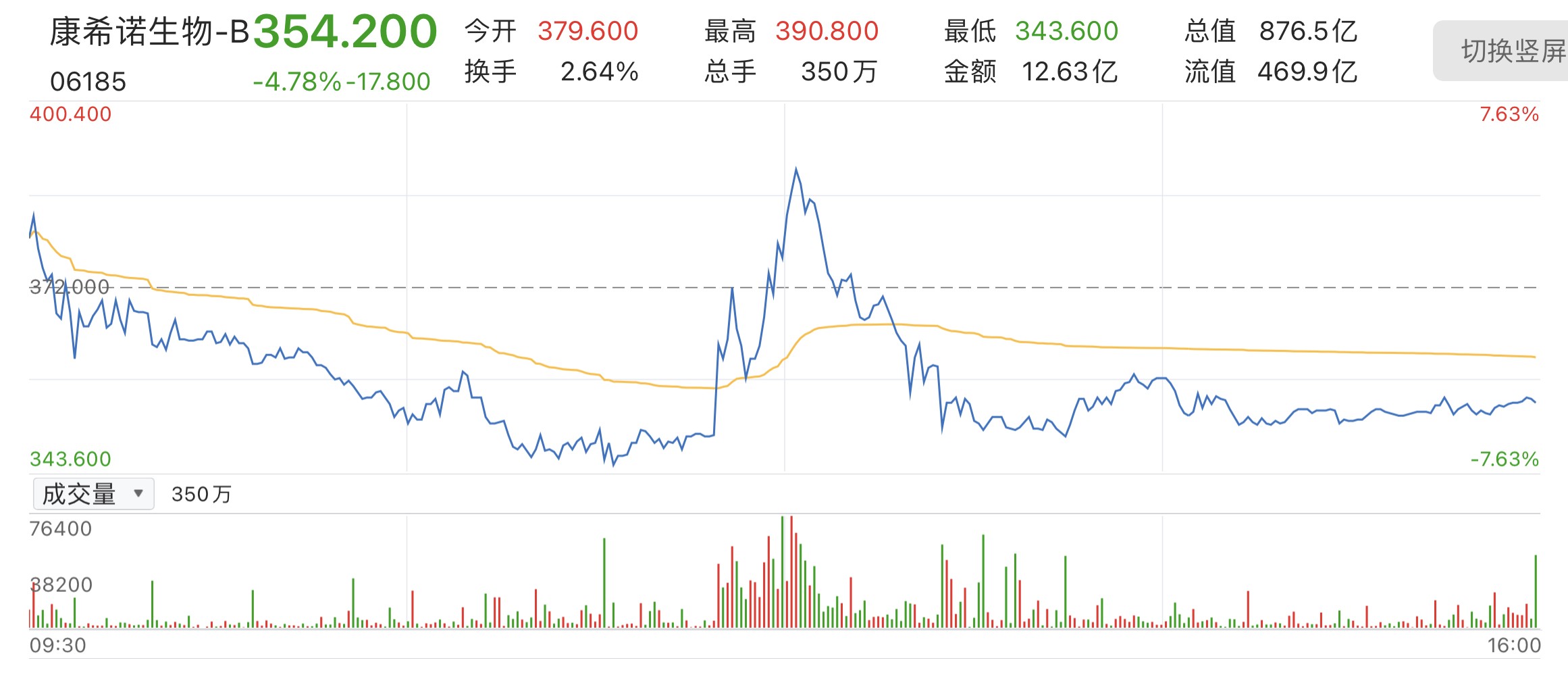
该公司午间于港股发布公告称,重组新型冠状病毒疫苗(5型腺病毒载体)附条件上市申请获国家药监局受理。
据介绍,康希诺与军事科学院军事医学研究院生物工程研究所陈薇院士团队共同开发的重组新型冠状病毒疫苗(5型腺病毒载体)(“Ad5-nCoV”,商品名为克威莎™),在巴基斯坦、墨西哥、俄罗斯、智利及阿根廷5个国家开展了全球多中心Ⅲ期临床研究,已完成4万余受试者的接种及期中数据分析。
结果显示:在单针接种疫苗28天后,疫苗对所有症状的总体保护效力为65.28%;在单针接种疫苗14天后,疫苗对所有症状总体保护效力为68.83%。疫苗对重症的保护效力分别为:单针接种疫苗28天后为90.07%;单针接种疫苗14天后为95.47%。
康希诺表示,Ad5-nCoV保护效力数据结果达到世界卫生组织相关技术标准及国家药品监督管理局印发的《新型冠状病毒预防用疫苗临床评价指导原则(试行)》中相关标准要求。2月21日,该公司已正式向国家药监局提交附条件上市申请,并获得受理。
此前康希诺曾透露,其研发的新冠疫苗接种一针即可提供保护力,目前该公司已经在中国开始一项两剂疫苗的临床试验,包括年龄在6至17岁和55岁以上的参与者。据悉,康希诺所研发的新冠疫苗储运条件也相对便捷,从目前的研究结果来看,在2到8℃条件下可稳定保存至少3个月,在25℃条件下可稳定保存至少2个月,在37℃条件下可稳定保存至少3周。
据公开信息,中国目前已经批准了包括国药中生以及科兴生物在内的两款新冠灭活疫苗,有效性在50%至91%之间。如果康希诺生物最终顺利获批,则意味着将成为国内获得附条件上市的第三款疫苗,也是国内获批的首款腺病毒载体新冠疫苗。
公开资料显示,康希诺专业从事高质量人用疫苗的研发、生产和商业化。2019年3月,康希诺生物在香港联交所主板H股上市;2020年8月13日,康希诺生物正式登陆科创版,成为科创板开板以来首只“A+H”疫苗股。
目前,康希诺研发产品仍未实现商业化变现,也未能实现盈利,成立以来持续处于研发中。财务数据显示,2016年至2019年,该公司归属于上市公司股东的净利润分别是亏损0.50亿元、亏损0.64亿元、亏损1.38亿元、亏损1.57亿元;期间的研发费用分别为6810万元、1.14亿元、1.52亿元。
1月28日晚间,康希诺披露业绩预告,预计2020年年度实现归属于母公司所有者净利润为-40,000.00 万元到-43,000.00 万元,与上年同期相比,亏损增加24,321.85万元到27,321.85万元,同比增加155.13%到174.27%。扣除非经常性损益后,其亏损额增至5.1亿元至5.4亿元,亏损幅度192.4%到209.6%。康希诺称,预计报告期内的研发费用为4.4亿元至4.7亿元,同比涨190%至209.7%。
不过,东兴证券、中泰证券等研究机构均认为,康希诺到2021年将迎来盈利。中泰证券此前研报认为,考虑新冠病毒疫苗2021年获批上市,预计康希诺2020-2022年归母净利润分别为-5.64亿元、19.82亿元和38.28亿元,分别同比增长-259.68%、451.51%、93.12%;若不考虑新冠病毒疫苗预计公司2020-2022年归母净利润分别为-0.95亿元、4.13亿元和7.81亿元,分别同比增长39.52%、535.40%、89.09%。
根据康希诺2020年中报,按销售收入计,国内的疫苗市场总规模由2014年的233亿元增至2019年的425亿元,预计到2030年将达到1320亿元,年均复合增长率为10.9%。此外,2019年,国内人均疫苗花费4.4美元,而美国的疫苗市场规模160亿美元、人均达57.7美元;康希诺认为“人均疫苗消费的巨大差距使得国内疫苗行业的发展具有巨大空间”。
界面新闻记者了解到,该公司逐步开展针对预防埃博拉病毒病、脑膜炎、新型冠状病毒(COVID-19)、百白破、肺炎、结核病、带状疱疹等13个适应症的16种创新疫苗产品的研发。康希诺2020年中报透露,除了公司预防脑膜炎球菌感染及埃博拉病毒病的3项临近商业化疫苗产品之外,公司有7种在研疫苗处于临床试验阶段或临床试验申请阶段,6种在研疫苗处于临床前阶段。

在2020年中报,康希诺称,公司拥有两款临近商业化的在研MCV产品;“国内的脑膜炎球菌疫苗市场将随着结合疫苗的推出而迅速增长,MCV2有望进入国家免疫规划成为免疫规划疫苗,MCV4则将在非免疫规划疫苗市场中占据较大市场份额”。灼识咨询测算预计国内脑膜炎球菌疫苗市场预计将由2019年的22亿元大幅增加至2030年的77亿元,年复合增长率为12.1%。兴业证券此前研报预计,这两款产品将于2021年获批上市。
2020年7月25日,康希诺宣布,已和辉瑞签署推广服务协议,其自主研发的四价脑膜炎球菌结合疫苗曼海欣(MCV4)获批上市后,将由辉瑞公司负责其在中国大陆市场的学术推广,合作期限最长为10年。这也是康希诺生物首款可能实现商业化的产品。
不过,研发风险仍不容忽视。东兴证券、兴业证券等多家机构均强调,警惕康希诺的新品研发风险及产品销售不达预期风险。兴业证券、中泰证券、国元证券还提醒投资者注意“疫苗黑天鹅事件”,比如:相关政策法规的变化及监管部门对疫苗行业监管力度加大的风险;疫苗上市后如出现不良事件、重大安全事件对康希诺持续经营带来的风险;以及市场空间不及预期的风险。




评论