界面新闻记者 |
界面新闻编辑 | 谢欣
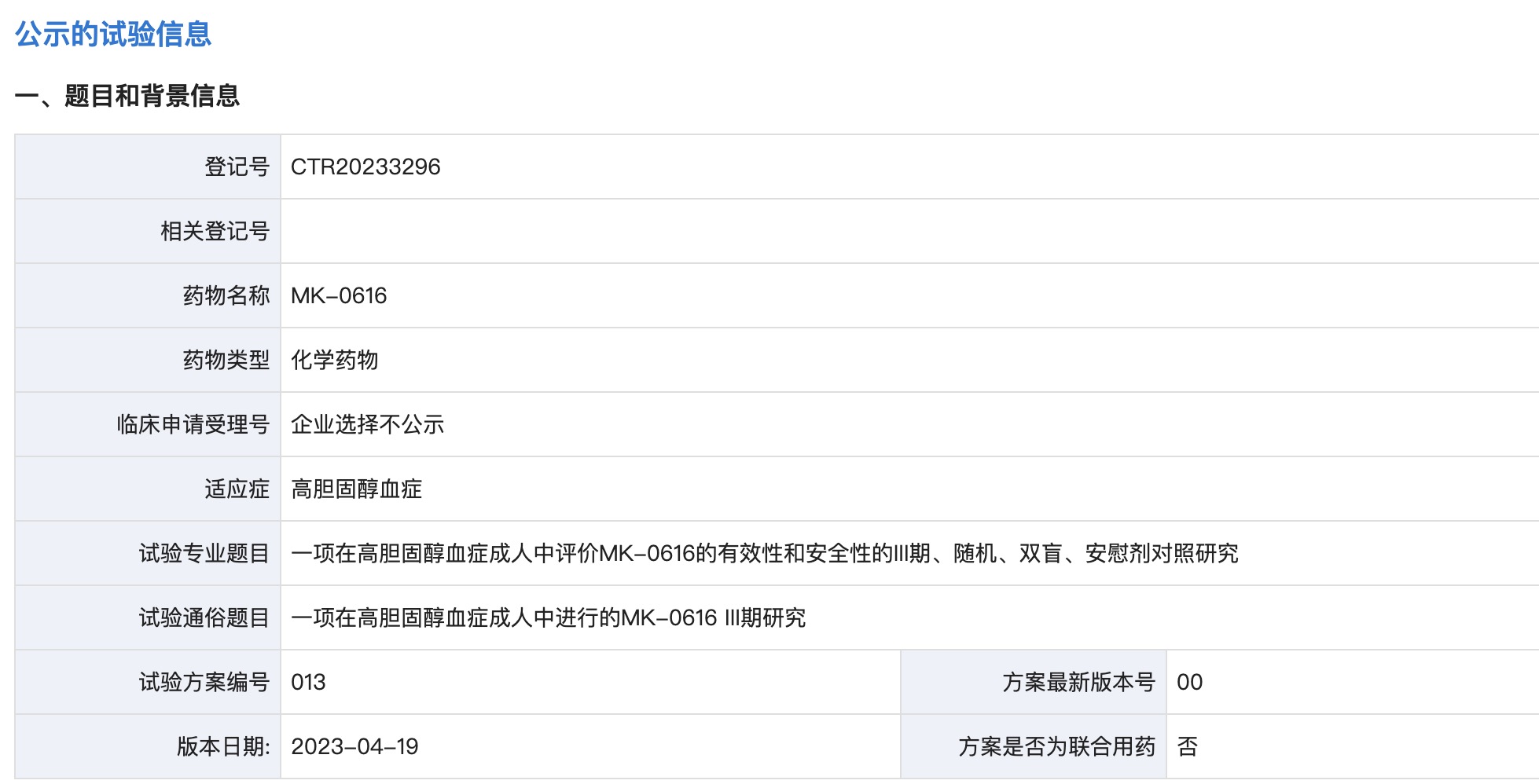
10月18日,国家药品监督管理局药品审评中心(CDE)官网公示,默沙东在中国启动了一项针对成人高胆固醇血症的名为“MK-0616”的口服PCSK9抑制剂的III期临床试验。
这是默沙东“MK-0616”国际多中心临床试验的中国区部分研究。据国家药品监督管理局药品审评中心官网,III期临床试验目标入组人数分别为国际2760人和中国 170人。
这也意味着,在国内PCSK9抑制剂这一降脂药热门领域,默沙东也即将入局。
 PCSK9抑制剂(前蛋白转化酶枯草溶菌素9/kexin9型抑制剂)是近年来发现以降低低密度脂蛋白胆固醇(LDL-C)为靶点的新型降血脂药。LDL-C被称为体内的“坏胆固醇”,它是导致动脉粥样硬化性心血管疾病(ASCVD)的主要原因。研究发现,降低LDL-C可以显著降低ASCVD的发病率和患者死亡风险。PCSK9抑制剂可阻止LDL受体降解促进LDL-C的清除,降低LDL-C水平。
PCSK9抑制剂(前蛋白转化酶枯草溶菌素9/kexin9型抑制剂)是近年来发现以降低低密度脂蛋白胆固醇(LDL-C)为靶点的新型降血脂药。LDL-C被称为体内的“坏胆固醇”,它是导致动脉粥样硬化性心血管疾病(ASCVD)的主要原因。研究发现,降低LDL-C可以显著降低ASCVD的发病率和患者死亡风险。PCSK9抑制剂可阻止LDL受体降解促进LDL-C的清除,降低LDL-C水平。
实际上,在今年3月,默沙东已披露在研口服PCSK9抑制剂MK-0616治疗成人高胆固醇血症患者的2b期临床试验的积极结果。该研究旨在评估4种不同剂量MK-0616(6、12、18和30mg)在患有高胆固醇血症的成人患者中的有效性和安全性。

据Insight数据库报道,该研究共入组381人,结果显示,在第8周,与安慰剂相比,所有剂量的MK-0616均显著降低了低密度脂蛋白胆固醇(LDL-C)水平,降幅从41.2%(6 mg,CI 95%:-47.8~-34.7;p <0.001)至60.9 %(30 mg,95% CI:-67.6~-54.3;p<0.001)。
截至目前,全球共有4款PCSK9抑制剂获批,包括3款PCSK9单抗,分别为赛诺菲/再生元联合研发的阿利西尤单抗注射液(Praluent)、安进的依洛尤单抗注射液(Repatha),信达的托莱西单抗。诺华的则是siRNA基因疗法药物英克司兰纳(Inclisiran)。
其中,诺华于2019年耗费97亿美金通过收购The Medicines获得的siRNA基因疗法药物英克司兰纳。英克司兰纳于2020年正式上市。界面新闻于今年4月曾报道,君实生物对诺华这一明星药发起专利无效请求。
阿利西尤单抗注射液和依洛尤单抗注射液是最早获批的两款PCSK9抑制剂产品,两者均于2015年获批,作用机理还是给药方式也均无明显差异。
2021年,阿利西尤单抗全球实现营收合计4.21亿美元,同比增长17%;2022年据再生元财报,阿利西尤单抗的销售额为4.67亿美元,增长率为10.93%。而安进的依洛尤单抗2021年全球销售额已突破10亿,实现营收11.17亿美元,同比增速高26%,不过在2022年增速有所降低至16%,但也达到12.96 亿美元的销售额。
实际上,在此之前,最早获批的两款PCSK9抑制剂也有过专利之争,安进与赛诺菲/再生元就PCSK9抑制剂打过一场反转不断的专利战。此后,又打起了价格战,安进在2018年10月宣布将产品降60%至5850美元/年。
与PCSK9单抗相比,诺华的英克司兰纳最大的特色则为,患者每年仅需两次皮下注射。而阿利西尤单抗注射液和依洛尤单抗注射液的使用频率为每两周皮下注射一次。此外,为了抢占中国市场,诺华也打起价格战,将英克司兰纳的价格降低到每针9988元,年治疗费用控制在2万元以内。
信达的托莱西单抗则于今年8月才刚获批上市。面对进口产品前后夹击的情况,前景仍不明确。
此外,前述已获批的4款PCSK9抑制剂均为皮下注射。而默沙东的MK-0616与前者们最大不同的是其为口服型,这提高用药方便和依从性为后续商业化埋下差异化的可能性,这或也是其落后仍继续推进研发的主要原因。
该领域也还有不少追赶者。据医药魔方NextPharma数据库,全球共披露了64个PCSK9研发项目。2016年前后是中国PCSK9项目立项的高峰期,如今跑在国内前列的项目有托莱西单抗(信达生物)、伊努西单抗(康方生物)、昂戈瑞西单抗(君实生物)以及recaticimab(恒瑞医药)。




评论